
近日,德国心血管器械公司百多力Biotronik宣布,其面向左束支区域起搏(LBBAP)的专用导线Solia CSP S 获得美国FDA批准。
Solia CSP S 是全球首款也是唯一将固定螺丝设计与导丝驱动植入方法相结合的起搏导线。其核心价值并不在“是否能做”,而在“是否更容易做、更多人能做”。
更值得关注的是时间窗口――在雅培与美敦力已经公布LBBAP相关临床积极结果、但尚未全面实现商业化的背景下,百多力率先获得FDA批准。这种领先并不只是上市节奏的差异,而更接近一次围绕技术路径的前置卡位。
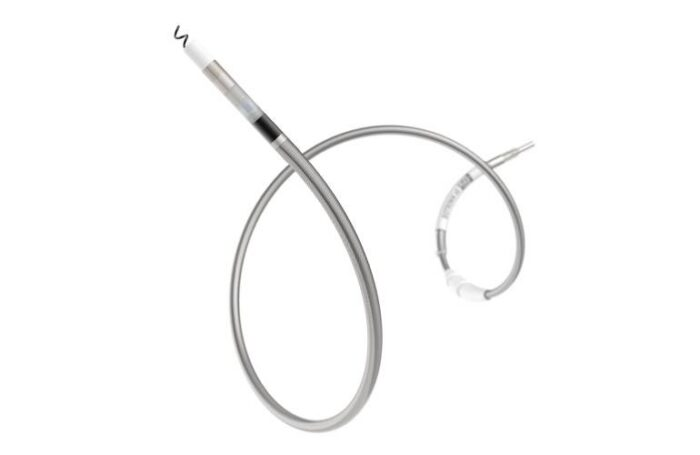
随着心脏起搏器治疗的发展,寻求最佳的生理性起搏方式成为当前研究的热点。
希氏-浦肯野系统(希浦系统)起搏,也被称为传导系统起搏(CSP),涵盖希氏束起搏(HBP)和左束支区域起搏(LBBAP)。这一方法只需通过一根电极连接到心脏自身的传导系统上,从而纠正束支传导阻滞,恢复心室收缩同步性,实现最接近生理状态的电传导。
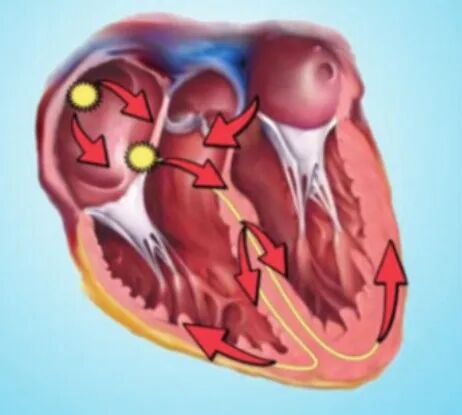
CSP起搏位点
然而,希氏束起搏手术目前面临一些挑战,其中手术成功率较低且操作难度较大。由于希氏束位于室间隔的膜部,存在耗电和电极易脱位等缺点。从临床反馈来看,LBBAP 起搏阈值更加稳定,植入成功率相对更高,同时学习曲线更具可控性,这些特征使其具备了向更大范围推广的潜力。因此,目前 CSP 手术以LBBAP 居多。
但问题在于,技术路径的成熟并未同步带来器械体系的完善。过去一段时间,LBBAP主要依赖传统主动固定导线配合导管系统来完成,医生需要在室间隔深部进行精细操作,这一过程高度依赖经验,也导致不同中心之间的成功率存在差异。这种“用旧工具做新手术”的模式,在早期探索阶段是可行的,但在走向规模化时会成为明显瓶颈。
因此,从2023年前后开始,行业逐步进入一个新的阶段,即从“术式驱动”转向“器械与术式协同驱动”。百多力此次获批的Solia CSP S,本质上正是这一趋势下的产物,其目标并不是创造一种全新的手术方式,而是将已有术式“工业化”。
# 竞争格局:百多力抢先,但真正的对手还在后面
从全球范围来看,LBBAP赛道仍然由传统起搏领域的三大巨头主导,即美敦力、雅培和百多力。三者在技术路径上的判断基本一致,均已围绕LBBAP展开布局。
已公开信息显示,雅培与美敦力在2025年前后均披露了其LBBAP系统的积极临床结果,说明其产品已进入临床验证的关键阶段。
美敦力OmniaSecure
OmniaSecure于2025年4月获批FDA,成为目前全球尺寸最小的经静脉除颤导线。该产品直径仅4.7法郎(约1.6mm,相当于木铅笔石墨芯的直径),旨在通过缩小导线体积降低静脉闭塞、三尖瓣反流等长期并发症风险,为心脏性猝死高风险患者提供更安全、持久的解决方案。

在2025年美国心律协会年会上,美敦力公布的LEADR LBBAP(左束支区域起搏除颤导线评估)研究晚期数据,以“100%除颤成功率+零严重并发症”的突破性成果,验证了全球最小直径除颤导线OmniaSecure在左束支区域植入的安全性与有效性。
LEADR LBBAP研究披露了以下数据:
-
除颤效能:超越预设标准,实现“零失败”记录。162例患者除颤测试:成功率达100%(预设疗效标准:88%),显著优于传统右心室起搏除颤系统(历史成功率约85%-92%);
-
除颤阈值稳定性:术后12个月内,平均除颤阈值波动范围<5%,远低于行业10%-15%的允许阈值,证明导线电学性能长期可靠。
-
手术安全性:零严重并发症,突破复杂植入技术瓶颈。前193例患者导线植入成功率:95.8%(按方案植入率,即未发生导线移位、定位失败等情况);
-
关键并发症零发生:未出现早期螺旋断裂、导线骨折、系统修订或死亡等与操作相关的严重并发症,远低于传统LBBAP手术约3%-5%的并发症率。
-
血流动力学改善:对比传统右心室起搏,LBBAP植入患者术后QRS波时限缩短约20%(反映心室同步性提升);
-
心功能保护潜力:初步数据显示,6个月随访期内,LBBAP组患者左心室射血分数(LVEF)下降幅度较对照组减少15%,提示对心衰进展的抑制作用。
雅培 Aveir CSP LP

Aveir CSP示意图
2025年美国心律协会年会上公布了全球首项针对LBBAP无导线起搏系统的首次人体临床试验结果。
该前瞻性急性可行性研究共纳入14例符合无导线起搏器植入指征的患者(平均年龄69.4±9.9岁,71.4%为男性),旨在评估新型无导线起搏器系统Aveir CSP LP实现LBBAP的急性安全性及技术可行性。
结果显示,有10名患者成功将Aveir CSP LP暂时植入心室间隔,其中5人达到左束支区域起搏标准(1人实现左束支直接捕获,4人为左室间隔起搏),另有3人表现为深间隔起搏,2人为右心室间隔起搏。起搏阈值为1.26±0.6 V(0.4 ms),R波幅值为10.2±4.1 mV,阻抗为373±56 Ω。手术总时长平均为48.1分钟,透视时长为15.9分钟。1个月内无严重设备不良事件的比例为85.7%。2例SADE分别为术中起搏器接触三尖瓣导致返流加重(未出现症状,保守治疗)及术后穿刺点血肿(不需手术干预)。
该研究证实Aveir CSP LP在结构上适用于左束支区域起搏,其延长电极螺旋能深入间隔达到LBBAP所需深度,且具备良好的电性能参数。虽然研究为急性试验,样本量有限,尚缺乏长期随访数据,但初步结果显示该系统具有良好的可行性、安全性及有效性,为后续临床研究奠定基础。
相比之下,百多力采取了更为渐进的路径:先在2024年通过Selectra 3D导管与Solia S导线获得适应症扩展,再在2026年推出明确针对LBBAP设计的专用导线。
这种路径差异,使百多力在当前阶段获得了一定先发优势。其可以更早进入美国市场,开展医生培训与术式推广,并在学术会议(如HRS年会)中建立影响力。但需要看到的是,这种优势更多体现在节奏上,而非决定性壁垒。
中长期来看,竞争的关键不在于“谁先获批”,而在于谁能够构建完整的解决方案体系。这不仅包括导线和导管,还涉及起搏器本体、算法优化(如自动阈值管理)、以及围绕术式的标准化工具。与此同时,临床数据的积累与指南地位的确立,以及医保支付体系的认可,也将成为决定市场格局的重要因素。

中国视角:LBBAP早已“临床领先”,但器械仍处早期
如果将这一进展放入中国市场背景,会呈现出一种结构性差异。中国在LBBAP的临床实践方面并不落后,甚至在部分研究领域具备一定领先优势。国内多中心研究已经在成功率、长期阈值等方面积累了较多数据,一些大型医院也已将LBBAP作为优先策略之一,这说明该术式在临床端的接受度正在快速提升。
然而,在器械层面,中国市场仍以传统导线与导管组合为主,整体仍停留在“非专用器械+术者经验”的阶段。这意味着,尽管术式本身已经具备推广基础,但其可复制性与标准化程度仍受到限制。从产业角度看,这是一种典型的“临床先行、器械滞后”状态。
# 监管对比:FDA进入“术式专用器械”,NMPA仍以适应症扩展为主?
从监管角度看,本次事件释放出的信号同样值得关注。FDA此次批准的是“明确为LBBAP设计”的专用导线,这在逻辑上不同于传统导线的通用属性,意味着监管机构正在接受“围绕特定术式定义器械”的审评路径。
相比之下,中国当前更常见的路径仍是基于既有产品进行适应症扩展,即在原有导线或导管基础上增加LBBAP使用场景。是否已经形成针对“LBBAP专用导线”的独立注册分类与技术审评标准,目前仍需进一步核实。这种差异如果持续存在,将对企业策略产生直接影响。
一方面,FDA路径更有利于细分创新产品的快速落地,有助于企业通过“first-in-class”建立技术标签;另一方面,NMPA路径则更偏向渐进式演化,有利于已有产品体系的延展。企业需要在两种路径之间做出取舍,或通过“双轨策略”进行布局。
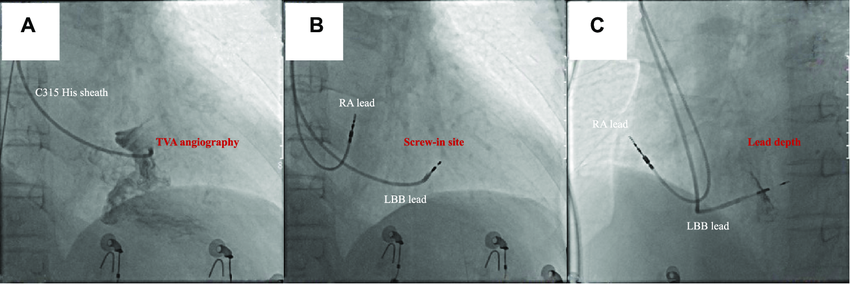
对中国企业的启示:不是“要不要做”,而是“什么时候做系统化”
百多力此次获批所传递的核心信息在于,LBBAP已经不再只是一个临床技术选择,而正在成为一个具备产业化潜力的细分赛道。在这一背景下,中国企业面临的问题,并非是否进入,而是如何进入。
首先,单一产品难以构建长期壁垒。未来竞争的核心,将不再停留在导线本身,而是围绕导线、导管系统、起搏器算法以及手术流程工具形成的整体解决方案。只有在这一层面建立能力,才能在高端市场中形成差异化。
其次,出海路径可能出现分化。一部分企业可能选择先在国内通过成本优势与临床推广建立基础,再逐步向海外拓展;另一部分企业则可能直接以FDA为突破口,开发差异化产品并建立国际标签。这两种路径各有优劣,也对应不同的发展阶段与资源禀赋。
进一步来看,LBBAP本质上是一个跨学科问题,涉及解剖结构、电生理机制以及器械工程设计的协同。谁能够在降低医生学习成本、提高一次成功率以及缩短手术时间方面取得突破,谁就更有可能在未来标准制定中占据主动。
# 心未来观察:从“医生技巧”到“工业产品”的转折点
百多力此次获得FDA批准,更像是一个阶段性标志。它所代表的,不只是一个新产品的上市,而是LBBAP从“依赖高手术者”向“依赖标准化器械”转变的开始。
类似的路径在医疗器械行业中并不罕见。无论是经导管主动脉瓣置换、电生理消融,还是腔镜手术设备,都经历过从术式探索走向器械主导的过程。当前的LBBAP,很可能正处在这一转折点上。
未来2至3年内,随着更多产品进入市场,临床证据逐步完善,以及指南与支付体系的跟进,该领域有望进入更清晰的商业化阶段。但与此同时,长期疗效数据、支付支持程度以及不同监管体系之间的差异,仍将构成不确定性来源。
在这些变量尚未完全明朗之前,可以确定的一点是:左束支区域起搏,正在从“技术可行”走向“产业成型”。而对于中国企业而言,真正的挑战,是在这一轮标准重构中找到自己的位置。
本站文章版权归原作者及原出处所有。内容为作者个人观点,并不代表本站赞同其观点和对其真实性负责,本站只提供参考并不构成任何投资及应用建议。本站是一个个人学习交流的平台,网站上部分文章为转载,并不用于任何商业目的,我们已经尽可能的对作者和来源进行了通告,但是能力有限或疏忽,造成漏登,请及时联系我们,我们将根据著作权人的要求,立即更正或者删除有关内容。本站拥有对此声明的最终解释权。声明:该文章系转载,登载该文章目的为更广泛的传递市场信息,不代表跟公司赞同其观点。文章内容仅供参考。
2026深圳国际心血管介入及技术展览会暨深圳国际心脏病学术会议将于12月9日-11日在深圳国际会展中心隆重举行,同时将组织深圳国际心脏病学术会议,诚邀您的参与展参展咨询热线:陆18930529086(微信同号)
深圳国际心脏病学术会议、心血管大会、心血管展会、医疗展、心血管介入展会、心血管技术展、2026深圳国际心血管介入及技术展览会、深圳国际心血管介入及技术展览会、心血管介入及技术展览会、深圳国际心血管介入大会、心血管病学术论坛、心血管病论坛、心血管护理论坛
展位预定:陆军(销售总监)手机/微信 18930529086 地址:上海市松江区莘砖公路668号双子楼A栋1003室
商务合作热线:万顺 总经理18616375066{不负责展位预定}© 2020 上海聚亿展览服务有限公司 沪ICP备14010562号-16 、上海隽博伟业展览服务有限公司 版权所有 沪ICP备2024101159号-1
深圳国际心脏病学术会议、心血管大会、心血管展会、医疗展、心血管介入展会、心血管技术展、2026深圳国际心血管介入及技术展览会、深圳国际心血管介入及技术展览会、心血管介入及技术展览会、深圳国际心血管介入大会、心血管病学术论坛、心血管病论坛、心血管护理论坛



 在线咨询
在线咨询

